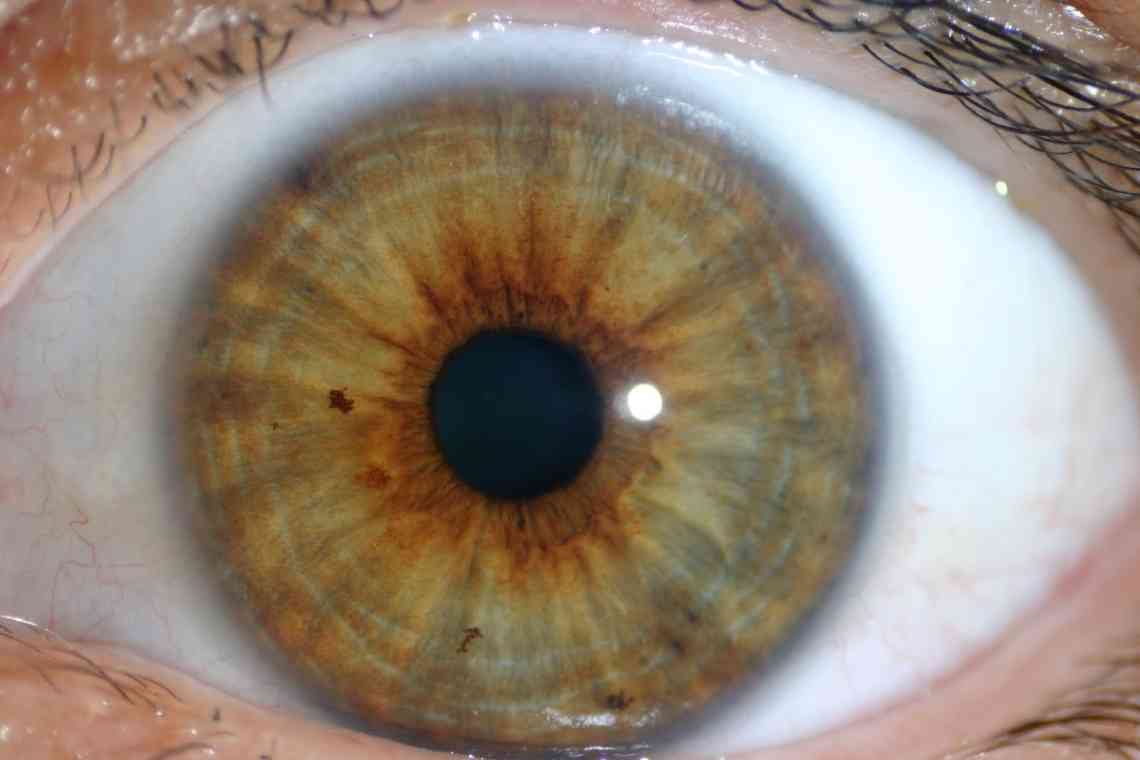
Псевдоексфоліативний синдром - це увеопатія, що характеризується відкладенням амілоїдоподібної речовини на структурах переднього сегмента очного яблука. Клінічна картина представлена зоровою дисфункцією, появою «помутнінь» і «райдужних кіл» перед очима, затуманенням зору. Діагностика базується на проведенні ультразвукової біомікроскопії, класичної біомікроскопії з використанням щілинної лампи, скополамінової проби, УЗД, візометрії, тонометрії, периметрії, гоніоскопії. Консервативна терапія ґрунтується на застосуванні антиоксидантів, антигіпоксантів, гіпотензивних засобів, вітамінів групи В, А, Е.
Загальна інформація
Псевдоексфоліативний синдром вперше був описаний фінським вченим Дж. Ліндбергом в 1917 році. Спостерігається взаємозв'язок між розвитком хвороби і віком пацієнта. У 50-59 років ймовірність виникнення патології становить 1-2,5%, у 60-69 років - 30%, після 70 років - 42%. Згідно зі статистичними даними, захворювання діагностується у 30% росіян старше 50 років. Ризик розвитку глаукоми у пацієнтів з псевдоексфоліативним синдромом дорівнює 64,6%. Патологія частіше зустрічається серед представників жіночої статі, проте важче протікає у чоловіків. Поширеність найбільш висока в серверних регіонах.
Псевдоексфоліативний синдром
Причини псевдоексфоліативного синдрому
Етіологія захворювання до кінця не вивчена. Тривалий час вчені пов'язували розвиток патології зі змінами будови епітелію кришталика, проте діагностика псевдоексфоліативного синдрому після інтракапсулярної екстракції катаракти дозволила спростувати цю теорію. На сьогоднішній день провідна роль у розвитку хвороби відводиться дії наступних факторів:
- Ультрафіолетове випромінювання. Вплив ультрафіолету індукує вільно-радикальне окислення і деструкцію клітинної мембрани. Це тягне за собою атрофію з типовими ознаками ексфоліації.
- Травматичне ушкодження. Травми очного яблука призводять до локальних змін, які у генетично скомпрометованих осіб є пусковим фактором пігментної дисперсії.
- Внутрішньоорбітальні інфекції. Багато авторів вважають, що поразка очей обумовлена підвищеною проникністю гематоофтальмічного бар'єру (ГОБ). Здатністю проникати через ГОБ наділена токсоплазма, вірус опоясуючого герпесу і краснухи.
- Порушення імунного статусу. На користь цієї етіологічної теорії псевдоексфоліативного синдрому свідчить виявлення в сльозній рідині підвищеної концентрації інтерлейкінів 6, 10, імуноглобуліну класу А і лактоферріну.
- Генетична схильність. У деяких пацієнтів можна встановити порушення експресії генів в ядрі і мітохондріях. Зустрічаність ПЕС серед родичів набагато вища, ніж у популяції. Простежується аутосомно-домінантний тип спадкування.
Вчені вважають, що розвитку хвороби сприяє куріння і аутоімунні патології. Вдається простежити взаємозв'язок між виникненням ПЕС і артеріальною гіпертензією, атеросклерозом, аневризмою аорти в анамнезі. Деякі дослідники вважають, що ці зміни - це наслідок системної васкулопатії, тому пацієнти з ПЕС часто страждають кардіоваскулярними захворюваннями.
Патогенез
Ключова роль у механізмі розвитку захворювання відводиться утворенню і депонуванню аномального екстрацелюлярного мікрофібрилярного білка на поверхні передньої капсули кришталика і райдужки, циліарному тілі, циннових зв'язках, по краю зірочного отвору. Рідше візуалізуються патологічні відкладення в області передньої камери. Встановлено, що білок належить до амілоїдоподібної субстанції, за його синтез відповідає пігментний епітелій і меланоцити райдужки. Згідно з сучасними уявленнями, патогенез ПЕМ пов'язаний з порушенням епітеліо-мезенхімальних взаємин у структурах очного яблука. Проникнення білкових структур в товщу його оболонок веде до їх дистрофічного переродження.
Псевдоексфоліативний синдром прийнято розглядати як системне порушення метаболізму сполучної тканини. Підтвердженням цієї теорії є виявлення специфічних відкладень у паренхіматозних органах (печінка, нирки, серце, головний мозок) і шкірних покривах. Вченими було виявлено 14 антигенів головного комплексу гістосумісності (HLA) при спадкованій формі патології. Прогресування захворювання веде до атрофії пігментної кайми, що проявляється вираженою дисперсією пігменту. Пігментоцити вдається виявити в КПК і на райдужній оболонці. Через ураження дренажної мережі порушується відтік водянистої вологи з подальшим підвищенням внутрішньоочного тиску.
Класифікація
В офтальмології розрізняють генетично детермінований та імуноопосередкований варіант розвитку. Незалежно від патогенезу хвороба завжди виникає в похилому віці. За вираженістю дистрофічних змін виділяють такі ступені псевдоексфоліативного синдрому:
- I - виявляється легкою атрофією райдужки. Патологічний процес не поширюється за межі кореня оболонки. Кайма зіниця має нерівномірну структуру. В області кришталика визначається маловиражене нашарування амілоїду.
- II - атрофія строми райдужної оболонки помірна. На поверхні райдужки і в зоні КПК виявляються виражені псевдоексфоліативні та пігментні відкладення.
- III - атрофічні зміни різко виражені. Пігментна кайма має вигляд «целофанової плівки», що обумовлено дисперсією пігменту. Ураження зв'язкового апарату викликає підвивих, рідше - вивих кришталика.
Клінічна класифікація базується на результатах ультразвукової біомікроскопії. Розрізняють наступні стадії патологічного процесу:
- I - ознаки поразки відповідають псевдоексфоліативному синдрому. Вдається візуалізувати точкові включення в передніх відділах очей.
- II - до вищеописаних змін приєднуються початкові ознаки пошкодження циннової зв'язки у вигляді чергування зон витончення з утовщенням. Довжина волокон різна.
- III - аномальні включення стають щільнішими, провокують руйнування зв'язкового апарату.
- IV - включення об'єднуються у великі конгломерати, які призводять до збільшення поздовжньої осі очного яблука за рахунок подовження переднього сегмента.
Симптоми псевдоексфоліативного синдрому
Для захворювання характерний тривалий безсимптомний перебіг. Спочатку вражається одне око (найчастіше ліве). Залучення другого очного яблука, як правило, спостерігається через 5-10 років після розвитку перших симптомів. Скарги зазвичай виникають вже після масивного відкладення амілоїду. Пацієнти відзначають появу «помутнів» перед очима. При погляді на джерело світла з'являються специфічні «райдужні кола». Зниження гостроти зору обумовлено ураженням кришталика, підвищенням ВГД і атрофією сфінктера райдужки. Порушується акомодаційна здатність, надалі розлади акомодації супроводжуються затуманенням зору, порушенням рефракції. Больовий синдром з'являється тільки при пошкодженні зв'язкового апарату.
Захворювання дуже повільно прогресує. Пацієнти часто ігнорують клінічні прояви. Крім скарг з боку очей при відкладенні білка у внутрішніх органах виникають симптоми їх ураження. При депонуванні амілоїда в печінці відзначається почуття тяжкості в правому підребер'ї, рідше - жовтяничність шкірних покривів. Біль у попереку за типом ниркової коліки, порушення сечовипускання є типовими ознаками скупчення білкових мас у паренхімі нирок. При поширенні патологічного процесу в товщу міокарда спостерігається відчуття здавлювання за грудиною, покалювання в області серця. Доведено, що ПЕМ широко поширена серед хворих на сенильну деменцію, когнітивні розлади, хронічну ішемію головного мозку, хворобу Альцгеймера.
Ускладнення
Відкладення білка в товщі кришталикових мас провокує розвиток вторинної катаракти ядерного типу, яка часто супроводжується слабкістю зв'язкового апарату. Це призводить до того, що більш ніж у половини хворих на катаракту виникає сублюксація, рідше - люксація кришталика. У більшості випадків патологія ускладнюється офтальмогіпертензією. Ураження трабекулярної мережі веде до виникнення псевдоексфоліативної відкритокутної глаукоми, а з прогресуванням захворювання - до глаукомної оптичної нейропатії або сліпоти. Поразка мейбомієвих залоз стає причиною ксерофтальмії.
Діагностика
Постановка діагнозу на доклінічній стадії ускладнена. Виявити перші ознаки можна тільки за допомогою ультразвукової біомікроскопії. Специфічні методи діагностики включають:
- Біомікроскопію ока. Дозволяє візуалізувати скупчення білого або сіроватого відтінку, що нагадує е пластівці на поверхні оболонок переднього відділу органу зору. Хаотичні скупчення пігменту можуть формувати веретено Крукенберга. Псевдоексфоліації за структурою схожі на запальні преципітати.
- Гоніоскопію. У передній камері визначаються множинні включення, які на пізніх стадіях формують великі конгломерати. При порушенні проникливості гематоофтальмічного бар'єру у водянистій вологі виявляється зважся крові. Об'єм камери не змінено.
- Безконтактну тонометрію. Характерно підвищення внутрішньоочного тиску, яке при вторинній глаукомі важко піддається зниженню медикаментозним шляхом. При ураженні дренажної системи додатково проводиться електронна тонографія.
- УЗИ очі. При використанні ультразвукової діагностики можна виявити розрив циннової зв'язки з виникненням сферофакії. Через масивні відкладення білка порушується співвідношення розмірів переднього і заднього сегментів. Методика також застосовується з метою обстеження заднього сегмента очей при зниженні прозорості оптичних середовищ.
- Ультразвукову біомікроскопію. Дає можливість виявити дрібноточкові включення слабкої акустичної щільності на оболонках ока, різницю довжини і лизис окремих волокон цинової зв'язки.
- Скопаламинову пробу. При 1 ступеня при проведенні проби зірочний отвір розширюється до 5 мм, при 2 - до 3,5-4 мм. При 3 ступені патології реакція зіниці відсутня.
- Візометрію. Зорова дисфункція спостерігається при помутненні оптичних середовищ або вторинній глаукомі. При важкому перебігу гострота зору знижується аж до світлодруження.
- Периметрію. Визначається концентричне звуження поля зору. У ряді випадків вдається діагностувати випадання окремих ділянок з зорових полів, скотоми.
Пацієнтам з даною патологією в анамнезі показана консультація невропатолога, ревматолога, кардіолога, гастроентеролога, отоларинголога. Необхідність проведення комплексного обстеження викликана системним ураженням фіброзної тканини. Часто виявлення перших симптомів ураження ока дозволяє діагностувати відкладення амілоїду в інших паренхіматозних органах.
Лікування псевдоексфоліативного синдрому
Етіотропна терапія псевдоексфоліативного синдрому не розроблена. Мета консервативного лікування - попередити розвиток важких ускладнень. На ранніх стадіях показано застосування:
- Антиоксидантів. Використовуються лікарські засоби, до складу яких входить супероксиддисмутаза. СОД належить до класу металопротеїдів. Антиоксиданти викликають руйнування активних форм кисню, які мають пошкоджувальний вплив на тканини ока.
- Антигіпоксантів. З метою поліпшення метаболізму і стимуляції процесу тканинного дихання застосовується цитохром С. Інстиляції препарату сприяють прискоренню епітелізації та репарації пошкоджень структур передніх сегментів очей.
- Гіпотензивних засобів. Показані при підвищенні внутрішньоочного тиску, ознаках офтальмогіпертензії і початкових стадіях розвитку псевдоексфоліативної глаукоми.
- Вітамінотерапії. Доведена ефективність застосування метилетилпіридінола (структурний аналог вітаміну В6), який володіє фібрінолітичною і антиоксидантною дією. В окислювально-відновлювальних процесах також бере участь вітамін А (ретинола ацетат) і Е (токоферола ацетат).
При тривалому перебігу патології метою лікування є усунення або зниження вираженості вторинних ускладнень. Медикаментозна терапія псевдоексфоліативної глаукоми часто не надає належного ефекту. Виникає необхідність у лазерному або хірургічному втручанні. Найбільш доцільно проведення ранньої лазерної трабекулопластики, проте через 3-4 роки виникають рецидиви підвищення ВГД. При виборі методу видалення сублюксованого кришталика слід віддавати перевагу факоемульсифікації. Методикою резерву залишається екстракапсулярна екстракція.
Прогноз і профілактика
Результат захворювання залежить від ступеня тяжкості, характеру ураження структур переднього відділу очей і типу ускладнень. При своєчасній діагностиці та лікуванні ускладнень прогноз щодо зорових функцій сприятливий. Виникнення вторинної глаукоми асоційовано з резистентністю до консервативної терапії та ризиком незворотної втрати зору. Специфічна профілактика не розроблена. Навіть при ранніх симптомах псевдоексфоліативного синдрому необхідна постановка на диспансерний облік у офтальмолога через високу ймовірність розвитку глаукоми. Показано регулярний контроль внутрішньоочного тиску. Хворі повинні проходити комплексне офтальмологічне обстеження не рідше, ніж двічі на рік.